Bạn đang xem bài viết Este là gì? Công thức cấu tạo, tính chất và phản ứng đặc trưng của Este tại vfu2.edu.vn bạn có thể truy cập nhanh thông tin cần thiết tại phần mục lục bài viết phía dưới.
Este là bài tiếp nối phần hóa hữu cơ của lớp 11, đồng thời cũng là mở đầu cho chương trình hóa học 12. Bài viết dưới đây Reviewedu sẽ chia sẻ tổng hợp các kiến thức hóa học về Este như: Este là gì? Công thức cấu tạo, tính chất hóa học, vật lý và phản ứng đặc trưng của Este, mời các bạn cùng tìm hiểu.
Este là gì? Công thức cấu tạo của este
Este là gì?
Este là một hợp chất hóa học được tạo thành sau khi thay nhóm -OH ở cacboxyl của axit cacboxylic bằng nhóm -OR’ của ancol.
Phân loại este
Dựa vào đặc điểm của gốc hidrocacbon và số nhóm Cacboxyl, Este sẽ được chia thành nhiều loại khác nhau như: Este no, Este không no, Este đơn chức, đa chức…
Công thức cấu tạo
Este có công thức tổng hợp chung là RCOO-R’

Riêng với Este no ta có công thức CnH2nO2 (n⩾ 2)
Trong đó:
- R là gốc hidrocacbon của axit
- R’ là gốc hidrocacbon của ancol (R’ khác H)
Tính chất vật lí của Este
- Trạng thái: Đa số ở trạng thái lỏng. Những Este có khối lượng phân tử rất lớn có thể ở trạng thái rắn (như mỡ động vật, sáp ong,…)
- Nhiệt độ sôi: Thấp, dễ bay hơi do không tạo liên kết Hidro giữa các phân tử.
- Tính tan: Ít tan hoặc không tan trong nước do không tạo liên kết Hidro giữa các phân tử với nước.
- Là dung môi để hòa tan các chất hữu cơ
- Hầu hết các este đều có mùi thơm riêng và rất đặc trưng như:CH3COOCH2CH2(CH3)2 có mùi chuối, Etyl butirat CH3CH2CH2COOC4H9 có mùi dứa,…
Phản ứng đặc trưng của Este
Phản ứng đặc trưng của Este là phản ứng thủy phân trong môi trường axit và thủy phân trong môi trường kiềm (phản ứng xà phòng hóa) xảy ra ở nhóm chức. Bên cạnh đó este còn có các tính chất của gốc axit và gốc ancol cấu tạo nên nó nên có các phản ứng khác như: phản ứng khử và phản ứng oxi hóa hoàn toàn.
Phản ứng ở nhóm chức
RyPhản ứng thủy phân trong môi trường axit
- Phương trình phản ứng:
- (COO)xyR′x + xyR↔yR(COOH)x + xR′(OH)y
Điều kiện
Môi trường thực hiện phản ứng thủy phân phải là axit loãng và được đun nóng.
Để tăng hiệu suất phản ứng thủy phân este thì phải dùng dư nước, thêm xúc tác là axit rồi đun nóng.
Trong phản ứng sinh ra Ancol không bền thì phản ứng thủy phân xảy ra một chiều.
- Phản ứng thủy phân trong môi trường kiềm (phản ứng xà phòng hóa)
- Phương trình phản ứng:
- Ry(COO)xyR′x + xyNaOH→yR(COONa)x + xR′(OH)y
Công thức
mchấtrắnsauphảnứng = mmuối + mkiềmdư
Số mol este phản ứng: nestephảnứng = nNaOHphảnứng = nmuối = nancol
- Phản ứng khử:Este bị khử bởi Liti nhôm hiđrua khi đó RCO– trở thành Ancol bậc I
- Phản ứng ở nhóm hidro
Este tham gia được nhiều phản ứng do có tính chất của gốc axit, trong đó phải kể đến phản ứng cộng với H2, Br2, Cl2,… giống Hidrocacbon không no và phản ứng trùng hợp của một số este đơn giản có liên kết C=C giống như Anken.
Ứng dụng của Este trong cuộc sống
Este có nhiều công dụng điển hình là:
- Làm dung môi để hòa tan các chất hữu cơ. Ví dụ: butyl và amyl axetat được dùng để pha sơn tổng hợp)
- Làm nguyên liệu sản xuất: Poli (metyl acrylat) và poli (metyl metacrylat) dùng làm thủy tinh hữu cơ. Poli (vinyl axetat) dùng làm chất dẻo, hoặc thủy phân thành poli (vinyl ancol) dùng làm keo dán. Một số este của axit phtalic được dùng làm chất hóa dẻo, làm dược phẩm.
- Một số este có mùi thơm của hoa quả được dùng trong công nghiệp thực phẩm (bánh kẹo, nước giải khát) và mỹ phẩm (xà phòng, nước hoa,…)
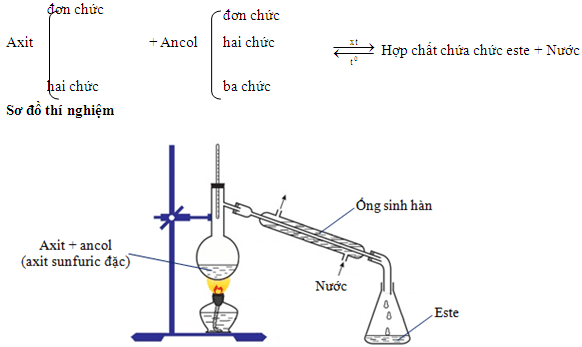
Các phương thức điều chế Este
Để điều chế Este có rất nhiều cách như: Thực hiện phản ứng este hóa giữa ancol và axit, phản ứng cộng giữa axit và hidrocacbon không no, phản ứng giữa muối Na của axit và dẫn xuất halogen, phản ứng giữa phenol và anhiđrit axit,…
Kết luận
Trên đây là tổng hợp một số kiến thức cơ bản về Este cần nắm để có thể làm bài tập và vận dụng tốt, làm nền tảng cho các bài hóa học về sau. Hy vọng rằng những chia sẻ của Reviewedu đã mang lại kiến thức hữu ích cho bạn.
Xem thêm:
Bia tiến sĩ được xây dựng để làm gì? Mục đích và thời gian xây dựng của bia tiến sĩ
Học ngành Kinh tế ra trường làm gì? Những công việc có thể làm sau khi tốt nghiệp ngành Kinh tế
Ngành Luật là gì? Học Luật ra làm gì? Cơ hội việc làm sau khi tốt nghiệp ngành Luật
Học công nghệ thông tin ra làm gì? Mức lương của ngành CNTT sau khi tốt nghiệp là bao nhiêu?
Ngành Marketing là gì? Học Marketing ra trường làm gì? Những trường đào tạo ngành Marketing tốt nhất
Học ngôn ngữ Anh ra làm gì? Học ở đâu và ra trường có dễ xin việc không?
Cảm ơn bạn đã xem bài viết Este là gì? Công thức cấu tạo, tính chất và phản ứng đặc trưng của Este tại vfu2.edu.vn bạn có thể bình luận, xem thêm các bài viết liên quan ở phía dưới và mong rằng sẽ giúp ích cho bạn những thông tin thú vị.
Nguồn: https://reviewedu.net/phan-ung-dac-trung-cua-este
Este là bài tiếp nối phần hóa hữu cơ của lớp 11, đồng thời cũng là mở đầu cho chương trình hóa học 12. Bài viết dưới đây Reviewedu sẽ chia sẻ tổng hợp các kiến thức hóa học về Este như: Este là gì? Công thức cấu tạo, tính chất hóa học, vật lý và phản ứng đặc trưng của Este, mời các bạn cùng tìm hiểu.
Este là gì? Công thức cấu tạo của este
Este là gì?
Este là một hợp chất hóa học được tạo thành sau khi thay nhóm -OH ở cacboxyl của axit cacboxylic bằng nhóm -OR’ của ancol.
Phân loại este
Dựa vào đặc điểm của gốc hidrocacbon và số nhóm Cacboxyl, Este sẽ được chia thành nhiều loại khác nhau như: Este no, Este không no, Este đơn chức, đa chức…
Công thức cấu tạo
Este có công thức tổng hợp chung là RCOO-R’

Riêng với Este no ta có công thức CnH2nO2 (n⩾ 2)
Trong đó:
- R là gốc hidrocacbon của axit
- R’ là gốc hidrocacbon của ancol (R’ khác H)
Tính chất vật lí của Este
- Trạng thái: Đa số ở trạng thái lỏng. Những Este có khối lượng phân tử rất lớn có thể ở trạng thái rắn (như mỡ động vật, sáp ong,…)
- Nhiệt độ sôi: Thấp, dễ bay hơi do không tạo liên kết Hidro giữa các phân tử.
- Tính tan: Ít tan hoặc không tan trong nước do không tạo liên kết Hidro giữa các phân tử với nước.
- Là dung môi để hòa tan các chất hữu cơ
- Hầu hết các este đều có mùi thơm riêng và rất đặc trưng như:CH3COOCH2CH2(CH3)2 có mùi chuối, Etyl butirat CH3CH2CH2COOC4H9 có mùi dứa,…
Phản ứng đặc trưng của Este
Phản ứng đặc trưng của Este là phản ứng thủy phân trong môi trường axit và thủy phân trong môi trường kiềm (phản ứng xà phòng hóa) xảy ra ở nhóm chức. Bên cạnh đó este còn có các tính chất của gốc axit và gốc ancol cấu tạo nên nó nên có các phản ứng khác như: phản ứng khử và phản ứng oxi hóa hoàn toàn.
Phản ứng ở nhóm chức
RyPhản ứng thủy phân trong môi trường axit
- Phương trình phản ứng:
- (COO)xyR′x + xyR↔yR(COOH)x + xR′(OH)y
Điều kiện
Môi trường thực hiện phản ứng thủy phân phải là axit loãng và được đun nóng.
Để tăng hiệu suất phản ứng thủy phân este thì phải dùng dư nước, thêm xúc tác là axit rồi đun nóng.
Trong phản ứng sinh ra Ancol không bền thì phản ứng thủy phân xảy ra một chiều.
- Phản ứng thủy phân trong môi trường kiềm (phản ứng xà phòng hóa)
- Phương trình phản ứng:
- Ry(COO)xyR′x + xyNaOH→yR(COONa)x + xR′(OH)y
Công thức
mchấtrắnsauphảnứng = mmuối + mkiềmdư
Số mol este phản ứng: nestephảnứng = nNaOHphảnứng = nmuối = nancol
- Phản ứng khử:Este bị khử bởi Liti nhôm hiđrua khi đó RCO– trở thành Ancol bậc I
- Phản ứng ở nhóm hidro
Este tham gia được nhiều phản ứng do có tính chất của gốc axit, trong đó phải kể đến phản ứng cộng với H2, Br2, Cl2,… giống Hidrocacbon không no và phản ứng trùng hợp của một số este đơn giản có liên kết C=C giống như Anken.
Ứng dụng của Este trong cuộc sống
Este có nhiều công dụng điển hình là:
- Làm dung môi để hòa tan các chất hữu cơ. Ví dụ: butyl và amyl axetat được dùng để pha sơn tổng hợp)
- Làm nguyên liệu sản xuất: Poli (metyl acrylat) và poli (metyl metacrylat) dùng làm thủy tinh hữu cơ. Poli (vinyl axetat) dùng làm chất dẻo, hoặc thủy phân thành poli (vinyl ancol) dùng làm keo dán. Một số este của axit phtalic được dùng làm chất hóa dẻo, làm dược phẩm.
- Một số este có mùi thơm của hoa quả được dùng trong công nghiệp thực phẩm (bánh kẹo, nước giải khát) và mỹ phẩm (xà phòng, nước hoa,…)
Các phương thức điều chế Este
Để điều chế Este có rất nhiều cách như: Thực hiện phản ứng este hóa giữa ancol và axit, phản ứng cộng giữa axit và hidrocacbon không no, phản ứng giữa muối Na của axit và dẫn xuất halogen, phản ứng giữa phenol và anhiđrit axit,…

Kết luận
Trên đây là tổng hợp một số kiến thức cơ bản về Este cần nắm để có thể làm bài tập và vận dụng tốt, làm nền tảng cho các bài hóa học về sau. Hy vọng rằng những chia sẻ của Reviewedu đã mang lại kiến thức hữu ích cho bạn.
Xem thêm:
Bia tiến sĩ được xây dựng để làm gì? Mục đích và thời gian xây dựng của bia tiến sĩ
Học ngành Kinh tế ra trường làm gì? Những công việc có thể làm sau khi tốt nghiệp ngành Kinh tế
Ngành Luật là gì? Học Luật ra làm gì? Cơ hội việc làm sau khi tốt nghiệp ngành Luật
Học công nghệ thông tin ra làm gì? Mức lương của ngành CNTT sau khi tốt nghiệp là bao nhiêu?
Ngành Marketing là gì? Học Marketing ra trường làm gì? Những trường đào tạo ngành Marketing tốt nhất
Học ngôn ngữ Anh ra làm gì? Học ở đâu và ra trường có dễ xin việc không?






